探索AKG在心血管疾病防治中的科學潛力
結論:AKG對心血管疾病積極意義,AKG****、改善動脈硬化、改善心肌缺血缺氧、改善心肌肥大、心肌梗死。
心血管疾病 (cardiovascular disease, CVD) 是50歲以上中老年人的常見病,是由心臟和血管發生病 理變化引起的多種疾病的總稱,包括***、外周 血管疾病和***等,具有高患病率、高致殘率和高死亡率的特點,臨床上表現為***、心肌缺血再灌注(MI/R) 損傷、心肌梗死 (MI)、心肌肥厚、心力衰竭 (HF)、擴張型心肌病、***等癥狀。流行病學統計的結果顯示,心血管疾病在全球流行病發病率排名中呈上升趨勢,居各種死因** 。2021年世界衛生組織的統計報告指出,心血管疾病在不同經濟體中的死亡率普遍呈上升趨勢(中高收入國家、中低收入國家、低收入國家) ;自2000年以來,全球心血管疾病死亡總人數增長了四分之一,*2019年因心血管疾病而死亡的人數就 已高達1790萬人 。
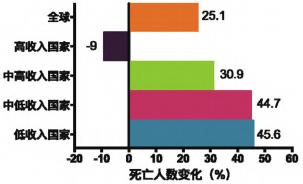
世界衛生組織2021年發布的報告顯示,心血管疾病在不同 經濟體中的死亡率普遍呈上升趨勢(中高收入國家、中低收 入國家、低收入國家);且自2000年以來,全球心血管疾病 死亡總人數增長了四分之一,2019年達到1790萬人。
2000?2019年心血管疾病死亡人數的變化(2021世界衛生組織統計報告)
1、AKG含量變化與心血管疾病
1.1 AKG的代謝及氧化應激
作為代謝過程中的關鍵分子,AKG既作為三羧酸循環的關鍵中間體參與碳水化合物的代謝過程,同時也作為連接細胞內碳-氮代謝的關鍵節點 影響氨基酸的代謝。AKG-既可以在α-酮戊二酸脫氫酶的作用下通過脫羧作用生成琥珀酸、水和二氧化碳,**終通過三羧酸循環徹底氧化分解;同時也能在谷氨酸脫氫酶的作用下與氨反應,轉化為谷氨酸,并進一步生成谷氨酰胺和谷胱甘肽。
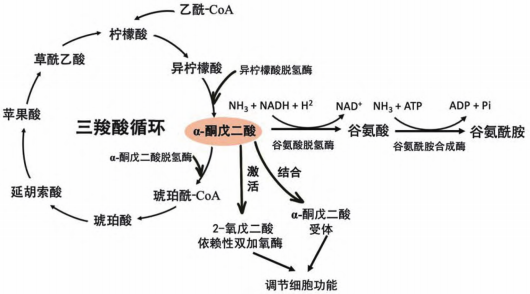
AKG既可以與氨反應,轉化為谷氨酸,并進一步生成谷氨酸和谷氨酰胺;也可以通過三羧酸循環生成琥珀酸、水和二氧化 碳。代謝產生的AKG可作用于AKG受體或***2-氧戊二酸依賴性雙加氧酶,進而發揮調節細胞功能的作用。
AKG的代謝過程與感應機制
AKG的感應機制比較復雜,不僅有多種胞漿和細胞核內感應蛋白可以進行特異性識別,也可以通過膜受體發揮作用。2- 氧戊二酸依賴性雙加氧酶 (2-OGDDs) 是一組系統發育上保守的酶,可催化各種類型的羥基化反應, 該酶在輔助因子Fe(II)存在時,通過O2和AKG作為共底物發揮作用。在人類中有超過60種 2-OGDDs,它們分別在缺氧反應、脂肪酸代謝、核酸修復和修飾以及表觀遺傳調控等生理過程中起關鍵作用。作為OGDDs的必需共底物,AKG對脯氨酰/天冬氨酰/賴氨酰羥基化產生影響,進而調節缺氧誘導因子HIF-1的穩定性和膠原合成。作為G蛋白偶聯受體(GPR99/GPR80/OXGR1)的配體,AKG也能通過G蛋白介導的信號通路***調節細胞功能。除上述感應機制外,研究人員在向成年秀麗隱桿線蟲飼喂AKG的過程中還發現一種新的AKG結合蛋白——ATP合成酶β亞單位,進一步揭示了AKG 所作用的調控網絡的復雜性。
作為一種潛在的**老分子和抗氧化劑,AKG能夠對抗細胞內氧化還原失衡,預防和*** 氧化應激引起的各種疾病。早在20世紀90年代,AKG就已憑借其在心肌能量代謝過程中的關鍵作用,引起了心臟外科手術**的關注。氧化應激增加是CVD常見的潛在病因之一,活性氧(reactive oxygen species, ROS) 增加不僅會導致一氧化氮可用性降低和血管收縮促進動脈***,同時也會導致 心律失常,ROS也會誘發***斑塊的形成。CVD患者常見血漿游離脂肪酸 (FFA)、膽 固醇或甘油三酯濃度升高,而AKG能夠抑制ROS的產生和預防脂質過氧化造成的損傷,降低哺乳動物體內膽固醇、LDL和甘油三酯的含量。 在心血管系統中,線粒體谷氨酸脫氫酶將AKG轉化為谷氨酸,谷氨酸對氧化應激有緩解作用,并通過增加三磷酸腺苷 (ATP) 來保護缺血心肌。不僅如此,研究發現在缺血缺氧小鼠體內AKG濃度明顯降低。作為心力衰竭的循環代謝標志物,AKG可能在心力衰竭的風險分層、預后評估和***指導中發揮特殊作用 ,有望成為臨床上心衰診斷和預后評估的標志物。
1.2 心血管疾病中AKG含量的變化
隨著年齡的增長,人類血漿中AKG的水平會下降 90%,膳食中補充這種代謝物是恢復其水平的***可行方法。衰老過程誘發心血管疾病的發生和發展,AKG 及其代謝過程中相關分子的水平可能與心血管疾病存在相關性。
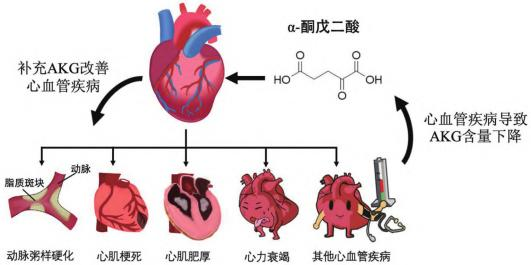
在不同CVD疾病模型中,AKG的含量普遍呈下降趨勢,回補AKG可有效逆轉這一趨勢并改善CVD的發生和發展。
圖:AKG含量與CVD之間的關系
Kjellman 等在心臟手術期間發現患者心肌的AKG含量非常低,且心肌中低含量的AKG會加重缺血性損傷。Kouou等的研究指出,缺血/再灌注 (I/R) 損傷影響大鼠心臟谷氨酰胺代謝,具體表現為谷氨酸和AKG含量的下降以及谷氨酸脫氫酶(GDH)活性的降低。I/R損傷組大鼠心肌AKG含量在損傷15 min后下降程度**為***,提前使用谷氨酰胺預處理則能***改善I/R大鼠的心臟功能。 在兔心肌缺血模型中,AKG含量在嚴重缺血時同樣呈下降趨勢。
心力衰竭的特點是能量需求和供應嚴重不平衡,心力衰竭發生時心臟ATP的可 用性降低30%~50%并逐漸無法維持心輸出量的要求。心力衰竭時,腎素-血管緊張素活性增強,心肌能量代謝異常,心肌能量消耗增加,因此有研究認為血清中的AKG含量可作為心力衰竭的生物標志物。 陳平安的研究發現AKG水平能反映心肌能量消耗水平,因此可以作為評估心肌能量消耗水平的血清標志物。心力衰竭患者的心臟組織中可見由慢性缺氧引起的線粒體異常。Lee 等發現在心力衰竭患者心肌組織分離的線粒體中,以AKG作為底物時的呼吸控制指數明顯較低。心力衰竭的發病機制與心肌細胞的代謝重塑密切相關。調節衰竭心臟中的谷氨酰胺代謝過程已成為***心力衰竭的新策略,作為一種代謝回補途徑,谷氨酰胺在谷丙轉氨 酶或谷氨酸脫氫酶的作用下分解為AKG后進入TCA循環。
AMP依賴的蛋白激酶 (AMPK) 與缺氧條件下血管內皮細胞的生成過程有關,其分為AMPK1α和AMPK2α兩個表型。研究發現,骨髓細胞特異性敲除AMPK2α的小鼠股動脈結扎后血流恢復受損超過80%。微陣列分析結果顯示,AMPK2α敲除小鼠的后肢中促血管生成相關蛋白的表達減弱。血管生成生長因子受缺氧誘導因子(HIF)的調控,AMPK2α通過調節AKG生成影響HIF-1α的羥化過程。缺氧引起的心肌細胞凋亡能減少AKG 的產生,進而可阻止HIF的羥基化和降解。Mühling 等通過超靈敏熒光高效液相色譜法觀察到暴露于低壓缺氧環境下長達3周的小鼠心室心肌中AKG濃度下降。
線粒體功能障礙在心肌梗死的病理過程中起著重要作用。Punithavathi 等在異丙腎上腺素誘導的大鼠心肌梗死模型中發現,經異丙腎上腺素處理后,大鼠心肌中線粒體脂質過氧化物的累積***增加,線粒體中異檸檬酸、琥珀酸、蘋果酸和AKG的含量***下降,NADH脫氫酶、細胞色素C氧化酶、琥珀酸脫氫酶、谷胱甘肽過氧化物酶和谷胱甘肽-S-轉移酶的活性***降低。
Watanabe等在探究谷氨酰胺代謝在氧化應激誘導的心肌衰竭中的調節機制時發現,經H2O2刺激后大鼠新生心肌細胞內的谷氨酰胺、谷氨酸和AKG水平***降低,且同位素示蹤結果顯示這一過程伴隨著谷氨酰胺酶上調。這表明在氧化應激條件下,心肌通過上調谷氨酰胺酶以補償AKG的損失及其向TCA循環的補充,并通過維持ATP和谷胱甘肽(GSH) 的水平抑制氧化應激從而發揮心臟保 護作用。
由環境因素和生活方式選擇引起的表觀遺傳畸變與心血管疾病的發生密切相關,如高脂飲食可能改變小鼠心臟DNA羥甲基化水平并導致AKG含量下降。Ciccarone等在高脂飲食飼喂8周和16周的小鼠心臟中觀察到DNA甲基化/ 羥甲基化修飾水平的改變以及DNA羥化酶Tet酶家族中Tet3的表達上調,此過程伴隨Tet的共底物AKG的含量***下降。
綜上所述,作為代謝途徑上的關鍵分子之一,AKG及其代謝過程中產生的相關分子的含量在不同心血管疾病模型中普遍呈下降趨勢。
2、AKG調節心血管疾病
2.1 AKG****
***又稱***癥,是指血中脂類含量(膽固醇、甘油三酯、磷脂、游離脂肪酸等)超過正常范圍的現象,它與心血管疾病的關系十分密切。
AKG參與調節脂質代謝,在降低體重、調節血漿低密度脂蛋白(LDL)和高密度脂蛋白(HDL)相對含量以及降低高膽固醇血癥的風險等方面具有一定積極作用。研究指出AKG可通過增強脂肪氧化來防止氧自由基生成和脂質過氧化損傷,從而使脂肪代謝正常化。
肉堿是協助脂肪酸進入線粒體的載體分子,線粒體外的脂質在肉堿脂酰基轉移酶的作用下進入線粒體并在線粒體內完成脂肪酸β氧化。有研究指出AKG參與肉堿的形成。降低AKG水平可能會升高乙酰輔酶A的水平,從而導致游離脂肪酸、 三酰甘油、膽固醇和磷脂的積累,補充AKG后脂質積累效應被逆轉。Radzki 等 指出,給予實驗性高膽固醇血癥模型大鼠不同濃度的AKG (分別為0.01 mol/L 和0.1 mol/L) 可降低血清總膽固醇、 LDL和甘油三酯的含量,升高HDL的含量,且AKG***組的體重***低于對照組。這些證據表明AKG可能對降低***風險具有一定臨床意義。
目前AKG已被申請專利作為降低血脂的藥物,用于***或預防脊椎動物,如鳥和人等哺乳動物血漿膽固醇、LDL和甘油三酯的升高并促進生成HDL。
2.2 AKG改善動脈硬化
***是一種慢性炎癥反應過程,是心血管疾病的主要病理學基礎,血管內皮功能障礙和炎癥是其發生和發展過程中的關鍵環節。動脈硬度與心血管危險因素相關,被認為是心血管疾病和衰老生物體死亡率的**預測因子。研究指出***患者和模式動物的血清和血管壁中通常存在過氧化脂質升高的現象,AKG 能夠抑制ROS的產生和預防脂質過氧化造成的損傷,并通過增加細胞代謝維持老年動物的血管彈性。
衰老動物彈性蛋白與平滑肌或膠原的比率降低是導致外周動脈硬化和相對阻力增加的原因之一。隨著年齡的增長,動脈壁的氧化應激增加,膠原合成過程及彈性蛋白的活性發生改變,**終導致主動脈壁變硬。AKG是脯氨酰-4-水解酶的輔助因子,由脯氨酰-4-水解酶催化形成的4-羥脯氨是膠原三螺旋形成所必需的物質。Niemiec等發現Ca-AKG顯著提高谷胱甘肽過氧化物酶活性,降低超氧化物歧化酶活性,并通過增加總膠原蛋白的含量改善血管硬化,證實了AKG對改善衰老動物血管彈性的積極作用。血管硬化與血管壁Ⅰ型和Ⅲ型膠原的異常積聚有關,脯氨酸在膠原合成中起關鍵作用,AKG誘導了脯氨酸合成。Harrison等指出AKG 通過誘導脯氨酸合成來逆轉或防止衰老動物的動脈硬化。
TET2 (ten-eleven-translocation oncogene family member 2) 是一種在進化上高度保守的去甲基化酶,也是一種依賴AKG和Fe2+的雙加氧酶,催化5-mC轉化為5-甲羥基胞嘧啶 (5-hmC),而DNA甲基化修飾異常與***的發***展密切相關。李榮慶的研究發現,相較于對照組,高脂飼喂的 ApoE-/-小鼠食用添加AKG的飼料后***斑塊數***減少,主動脈竇部的膠原纖維含量明顯下降。該研究進一步指出,AKG通過TET2上調血管內皮細胞的自噬及自噬流來抑制炎癥因子表達,延緩***的發生和發展。
2.3 AKG改善心肌缺血缺氧
心肌缺氧(myocardial anoxia)引起心肌供血不足,臨床上表現為冠狀動脈血流量降低、心肌氧供應不足等癥狀。體外研究結果顯示補充AKG明顯緩解缺氧誘導的損傷,而同時補充亮氨酸和 AKG 能顯著提高心臟指數,減少外界不良因素對心臟的損傷,促進心臟生長。Tkachenko等評估了AKG對異丙腎上腺素誘導的心肌損傷大鼠的保護作用,結果顯示AKG通過減少氧化應激和調節抗氧化系統的活性緩解了大鼠心肌的缺血程度。
臨床研究發現高濃度的AKG能夠***改善冠 狀動脈手術患者的心肌功能,該保護作用可能與AKG的氧化作用有關。Kjellman等在接受心臟手術的46~78歲男性中發現,心臟停搏期間提供高濃度的AKG減輕了患者術后心臟缺血的跡象,改善了心肌功能,患者血漿中的缺血標志物血漿肌酸激酶同工酶MB(CK-MB) 和肌鈣蛋白T***減少,術后未檢測到AKG對血壓的不良影響。富含AKG的含血停搏液可以減輕心臟停搏主動脈阻斷和早期再灌注時心肌底物代謝的異常 。
心肌梗死是指由動脈內壁中形成斑塊導致流向心臟的血流減少和心肌缺氧,**終損傷心肌的一種疾病,是心血管疾病的臨床表現之一。Tishkin等在心肌梗死大鼠模型中評估了AKG的抗缺血能力及其對心肌氧化過程的影響,結果發現 AKG具有***的心臟保護功能,且這一功能與糖酵解和肌酸激酶系統的酶活化過程中的能量轉運有關。研究發現高心臟負荷時細胞通過糖酵解補充能量,并生成ATP、細胞溶質NADH及**酸,在這一過程中糖酵解的還原當量通過線粒體AKG與胞漿蘋果酸的交換進入線粒體。
Russ等在阻斷冠狀動脈誘導的Wistar大鼠心肌梗死模型和過氧化氫誘導的雞心組織氧化模型中,探究了一種由AKG 、5-羥甲基糠醛、N-乙酰-硒-L-蛋氨酸和N-乙酰-L-蛋氨酸幾種活性成分組成的多組分溶液在心臟組織中的抗氧化能力,結果發現這種多組分溶液在兩種動物模型的心臟組織中均起到緩解氧化應激的作用,并改善冠狀動脈閉塞的情況,其中AKG被鑒定為該多組分溶液中的有 效抗氧化成分。經AKG處理后,心臟組織中的氧化應激標記物丙二醛 (MDA)和羰基蛋白(CPs)水平恢復到損傷前水平。事實上,大量實驗均已證實了AKG的抗氧化作用。Watanabe等發現二甲基 AKG 可以改善H2O2刺激后的大鼠新生心肌細胞內ATP和GSH的水平,同時抑制氧化應激誘導的細胞凋亡。
心肌缺血時間有限是限制心臟移植的**重要因素之一,主動脈交叉夾會導致缺血再灌流(I/R)損傷,臨床上使用停搏液在體外循環期間保護心臟***功能。組氨酸-色氨酸-AKG溶液(histidine-tryptophan- ketoglutarate solution, HTK 溶液)是先天性心臟手術常用的停搏液。Hachida 等觀察了AKG和色氨酸對保存6小時后心功能恢復的影響,結果發現相較于對照組,去除AKG的HTK溶液處理組的血壓***降低、釋放酶 (CK-MB)升高 (P < 0.01),但冠脈流量無明顯變化;在去除色氨酸的HTK溶液處理組中*發現血壓和冠狀動脈血流百分比的***下降 (P < 0.01)。因此,研究者們推測AKG與色氨酸聯合使用對缺血心肌具有更***的保護作用。臨床研究證實HTK溶液具有保護冠狀動脈皮下細胞組織、恢復嬰幼兒心臟手術中主動脈開放后自動復跳率等功能。Arslan等的研究表明,使用低劑量 HTK進行短時間鉗夾手術可以起到與晶體性心臟停搏液一樣的心肌保護效果。
2.4 AKG改善心肌肥大
病理性心臟肥大通常由***、心臟瓣膜病、心肌梗死和神經***等壓力刺激和疾病誘導。持續的病理性肥大反應會導致心肌收縮功能障礙和心力衰竭。心肌肥厚和充血性心力衰竭患者體內可以觀察到糖酵解的增加,增加果糖2,6二磷酸可抑制小鼠模型的心肌肥大。Liang等發現AKG可以抑制苯腎上腺素灌注所致的心肌肥大小鼠心肌細胞中的[3H]-亮氨酸攝取,表現出一定的抗心臟肥大的作用。
An等發現補充 AKG可抑制壓力超負荷引起的心肌肥厚及心臟功能障礙,并抑制壓力超負荷條件下的心肌纖維化,且對左心室功能無明顯不良影響。研究結果顯示,連續9周服用含有2%AKG水溶液的小鼠平均心肌細胞橫截面積減少 49.11% (P < 0.001),肌球蛋白重鏈7 (Myh7)、心房利鈉因子(Nppa)等心臟肥大標志物的mRNA和蛋白水平均***降低,AKG抑制了橫斷主動脈縮窄小鼠心 肌TGF-β1的過度表達。體外實驗進一步證明AKG通過降低血管緊張素II (Ang II)誘導的β-MHC和ANP上調來修復Ang II介導的線粒體膜電位損傷,從而減少心肌細胞凋亡。研究發現AKG通過調控PINK1/Parkin 通路促進線粒體自噬相關蛋白的表達量增加,降低ROS水平,表明AKG可能通過增強有絲分裂期間細胞的吞噬功能來***受損的線粒體DNA,從而減輕壓力超負荷下的心肌氧化應激。
事實上,過度自噬介導的致病性細胞重塑是壓力超負荷引起的擴張型心肌病的發病機制之一。 Mari?o等發現AKG衍生物二甲基α-酮戊二酸(DMKG)可作為一種自噬抑制劑***擴張型心肌病。該研究發現,抑制糖酵解、脂肪酸氧化等過程 導致的AcCoA水平降低會誘導自噬,補充AcCoA則會抑制自噬。持續補充 DMKG可以增加細胞溶質中AKG的濃度,升高AcCoA水平,從而調節自噬過程,改善心肌自噬導致的胸主動脈縮窄反應,緩解左心室擴張和心肌收縮性能降低等癥狀,消除心肌細胞肥大與心肌細胞纖維化,實現防治擴張性心肌病的目的。
AKG的受體氧戊二酸受體1 (OXGR1)是G蛋白偶聯受體(GPCR)蛋白家族成員之一,GPCR通常被認為在調節心血管疾病中發揮重要作用。Omede等發現 OXGR1基因敲除的小鼠橫向主動脈縮窄導致心肌肥厚***增加,心臟收縮功能減弱,心臟射血分數***降低。進一步的研究顯示,OXGR1可能與COP9信號體復合物亞單位5 (CSN5)形成復合物,然后在上游調節因子TYK2的作用下抑制STAT3***,從而調控心肌肥厚;而OXGR1的缺失則導致STAT3過度磷酸化,加重心臟肥大。這一研究揭示了AKG受體OXGR1在調節心臟功能中 的作用。
2.5 AKG在其他心血管疾病中的功能
心臟交替(cardiac alternans)與快速室上心律失常和心源性猝死的發生有關,研究表明肌漿網Ca2+- ATP酶2a (SERCA2a)上調改善代謝抑制誘導的細胞交替。Stary在探究線粒體功能受損對細 胞交替的影響的過程中發現,不論是對照組還是SERCA2a過表達組小鼠,阻斷AKG脫氫酶的功能時,交替程度均明顯增加。Nelson等的研究認為AKG與亞臨床心房功能障礙和心源性栓塞卒中 有關。
心臟祖細胞 (CPCs) 自體移植可以減輕受損心臟的心肌功能障礙。Salabei等評估了谷氨酰 胺對CPC增殖的調控作用,結果發現谷氨酰胺通過轉化為AKG促進CPC的增殖作用,并促進TORC1底物p70S6k以及視網膜母細胞瘤蛋白的快速磷酸化,誘導細胞周期蛋白D1和CDK4的表達;補充谷氨酸鹽和細胞通透性AKG (DMKG)均增加了細胞耗氧率,DMKG增加了線粒體氧化磷酸化解偶聯劑FCCP刺激的呼吸速率,且mTORC1信號觸發的AKG是CPC增殖能力的主要決定因素,證實了AKG在CPC細胞增殖過程中的重要作用。
人心肌間充質細胞(CMSCs)在適當的條件下能夠重新定向分化為心肌細胞,因此被認為對心臟修復***具有可觀的前景。Spallotta等通過代謝組學分析發現,糖尿病患者的CMSCs及HFD小鼠整個心臟的細胞內AKG合成減少。外源補充AKG則拯救了心肌間充質細胞的功能并改善其增殖能力。此外,給予外源 AKG補充后,糖尿病患者的CMSCs的線粒體融合數***增加,功能也明顯改善。
Ogiso等在給血壓正常的大鼠靜脈注射AKG后發現,10 mg/kg的AKG具有一定的***作用。
Ba?ramkulov等則評估了AKG和琥珀酸對犬缺血心肌的側支冠狀動脈循環 (CCC)的影響,結果發現AKG (6mg/kg冠狀動脈內和60 mg/kg 靜脈內)對犬 CCC和心肌的收縮活性具有一定的改善作用。靜脈注射 AKG (12 mg/kg)和琥珀酸鹽 (100 mg/kg)可***降低結扎引起缺血的心肌中的葡萄糖消耗,證明一定量的AKG和琥珀酸可用于CCC的校正和缺血心肌的能量供應。
**物誘導氧化應激,導致神經毒性、脂質過氧化和膜功能障礙,并***抑制抗氧化功能,如降低SOD活性和GSH水平。AKG是一種有效的**物致死拮抗劑,能改善**物導致的心血管損傷。AKG還可以還原心肌細胞中的細胞色素C,并保護**物損傷模型中心臟和肝臟線粒體中的氧化磷酸化和細胞色素C氧化酶(Cox)的活性。
3、總結與展望
作為生物代謝過程中的重要中間體,AKG和細胞的合成與分解聯系密切。針對 AKG的生物學特征,科學家們開發出了AKG的多種功能并將其應用于傷口愈合、心臟保護等多種場合。不僅如此,AKG在腸道、脾胃、肝臟、心臟、眼等組織的相關疾病,甚至**的***過程中也表現出了一定的應用價值。
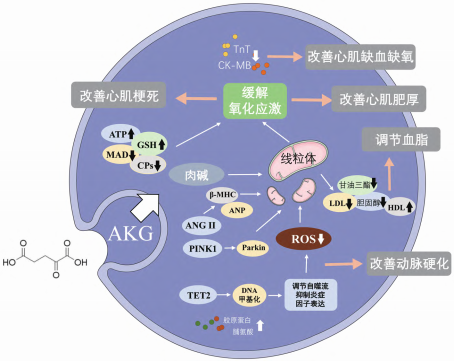
AKG調節心血管疾病的分子機制
AKG還可以調節生物體的衰老過程,延長不同動物的壽命,這為科學家們對 AKG應用的研究提供了新的思路。作為一種極具潛力的膳食補充劑,美國食品藥品監督管理(FDA)認為其符合公認安全(generally recognized as safe, GRAS)等級,目前關于AKG在人體中的研究正在開展中。值得一提的是,大多數的人體試驗及市面上的配方大多將AKG和氨基酸混合在一起,AKG自身的功效亟待開發。
心臟功能的穩定對生命體的健康發展至關重要。CVD作為全球流行病致死率比較高的疾病,如何改善和***該疾病是科學家們試圖研究和解決的問題。目前*** CVD的手段主要包括藥物***、基因編輯、細胞療法等。AKG作為生物體自身 細胞新陳代謝過程中產生的重要中間體,相較于其他***CVD的藥物具有毒性低、副作用小等優點。不僅如此,AKG具有良好的溶解性,在水溶液中相對穩定并可被人體完全代謝。AKG14C標記實驗顯示,服用該化合物3 h后,肝臟、大腦、皮膚、肌肉和骨組織組織中均已經存在被標記的AKG。大量研究證實,在不同心血管疾病模型中,AKG及其代謝過程中產生的化合物的含量均發生了不同程度的改變,AKG在CVD中扮演的角色還有待進一步探索。研究指出,AKG受體OXGR1可能作為一種調節因子在壓力超負荷誘導心肌肥厚中發揮作用,但改變OXGR1的表達是否會影響心肌生長和重塑仍有待研究,OXGR1很可能在未來成為一種新的***靶點。
本文就AKG在CVD中的特征及功能進行了綜述。AKG通過抗氧化、***、調節免疫系統等方式,保護心肌功能,調節心肌梗死、心肌肥大、心力衰竭等心血管疾病的發生和發展,同時在調節血壓血脂、改善動脈硬化等過程中也發揮了一定的積極作用,證實了AKG在***心血管疾病方面具有可觀的潛在價值,但 AKG保護心血管疾病作用的具體機制研究還較少。值得一提的是,由于腸內 AKG在胃和十二指腸被吸收或代謝,或被胃中的微生物代謝,導致周圍組織對 AKG的利用率低,因此如何提高AKG的利用率以及AKG在人體內的營養比較好需要量這一問題也亟待研究。總而言之,作為一種膳食補充劑,可以預見AKG 在預防和***心血管疾病方面極具開發潛力。



